医疗设备CE-MDR认证标签上应注明哪些信息?
医疗设备CE认证标签上应注明哪些信息?
《医疗器械法规》(MDR)不久将适用,并将要求在医疗器械标签上注明各种信息。制造商如何在短期内以协调的方式遵守这些要求?
欧洲拥有24种官方语言,因此必须使用符号来传达标签上的所需信息。MDR的附件I第三章23.2规定了标签必须包含哪些信息,从简单的“医疗设备”到UDI承运人。MDR允许在标签上使用符号代替书面语言(附件I,第三章,23.1.h)。
信息量很大,可以减轻制造商的工作负担MedTech Europe已发布了符号设计,标题和翻译,并建议在国际上使用它们。但是,必须在与MDR 23.1.H一致的使用说明书中对其进行描述,直到未在统一标准中发布它们为止。
如果特殊情况需要,鼓励制造商使用以下符号,始终以如下所示的顺序使用 -旨在加快用户对符号及其含义的认识和接受。
欧洲医疗技术提议的符号设计:
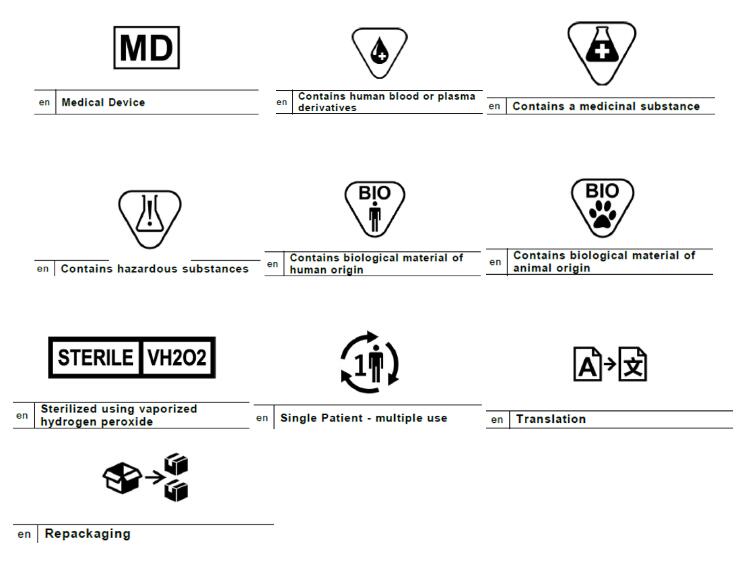
此外,作为文本的替代,还建议在植入卡上使用以下符号(MDR第18条):










