第16页
-
电池和蓄电池指令2006/66/EC限值要求
欧盟委员会(EC)发布了欧盟电池指令2006/66 / EC的修正案(修正案2013/56 / EU),该修正案禁止在欧盟使用含汞纽扣电池,以鼓励市场上销售含汞的纽扣电池含有较少的污染物质。自2015年10月1日起,纽扣电池中的汞(Hg)限值将从原来的2%降低至0.0005%。欧盟委员会将审查可满足降低汞限值的纽扣电池的可用性,并决定是否豁免应扩大。2006/66/EC指令的重点:1.修订了电池中汞和镉的使用限制;2.新电池的标签要求,以帮助消费者选择和回收;3.修订的铅,汞...
-
关于MDR法规2017/745:主要变化是什么?
关于医疗器械的第2017/745号法规将于2021年5月26日生效。由于Covid-19大流行,该法规的第一个截止日期推迟了一年,从那时起,它将对各经济运营商施加新的义务。医疗设备行业。这里是要记住的要点的快速摘要。关于此医疗器械新法规要记住的要点:1.适用范围与旧指令相比,新医疗器械法规的适用范围得到了扩展。确实,非医疗设备现在已包含在该法规中,并在附录XVI中列出。此外,您的医疗设备的分类可能会改变。指令列出了56条标准的18条规则,而该法规包括22条规则和80条标准。这意味着设备可以从一类转移到另一类,尤其是...
-
欧盟托运的授权欧盟代表要求
昨天,我从一个潜在客户那里提出了一个问题,该问题涉及欧盟货运的授权代表的要求。为了避免混淆,我们始终将其称为我们的欧盟授权代表。客户阅读了一篇参考欧洲法规的文章,该法规似乎要求所有欧盟出口商都必须指定一位授权的欧盟代表。那是不准确的。该法规是(EU)2019/1020法规。在昨天之前,我从未听说过它。不用担心……我阅读了全部44页,因此您不必阅读。概要概要是这样的:您不受(EU)2019/1020法规的约束,但是在欧盟境内处理您的产品的人受此约束。您必须真诚地为他们提供帮助...
-
欧盟FCM政策修订路线图
欧盟委员会DGSANTE出版了《初始影响评估》,作为修订欧盟食品接触材料法规的路线图;概述了在持续评估过程中确定的八个主要“问题”,以及计划的影响评估应考虑的可能政策选择;评论期开放至2021年1月29日。2020年12月18日,欧盟委员会(EC)健康与食品安全总局(DGSANTE)就其初始影响评估(IIA,本质上是扩展路线图)开展了磋商,以持续评估和修订欧盟法规食品接触材料(FCM)上。咨询开放至1月29日,2021年DGSANTE将举办一个网络研讨会提出关于2021年1月20,路线图。背景内容: &...
-
什么是UKCA标志?
什么是UKCA标志? UKCA标志UKCA标记(UK Conformity Assessed标记)是英国在英国(英格兰,苏格兰和威尔士)投放市场的产品所需要的英国产品标记要求,取代了欧盟对CE标记的要求(CE标记将继续是在北爱尔兰接受)。UKCA标记将表明在英国市场上投放的产品符合UKCA标记要求。UKCA标记是在原始的“欧盟出口”英国法定文书中指定的,并且对于大多数产品,这是在英国法定文书2019年第696号及其修订中定义的(例如,汽车,船舶和医疗设备除外)。“欧盟出口”英...
-
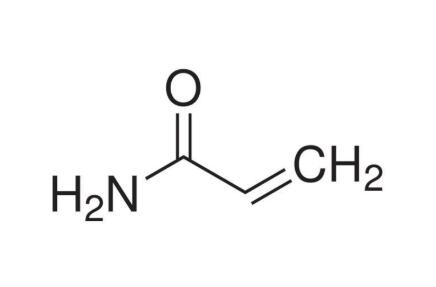
丙烯酰胺分析_高分子化学测试_化学痕量分析
在化学品,食品和其他材料中进行丙烯酰胺测试和分析。商通检测为质量控制应用和法规要求提供丙烯酰胺测试实验室支持。丙烯酰胺测试包括纯度,组成和法规分析。商通检测提供的各种分析仪器,丙烯酰胺的检测和测试可以达到痕量ppm水平,甚至更低。液相色谱-质谱(LC-MS),气相色谱-质谱(GC-MS)等。丙烯酰胺测试与分析:1.化学痕量分析工业化学痕量分析测试,涵盖未知物和痕量残留物的识别,污染检测和法医分析对准确的化学痕量分析的需求对于解决行业问题至关重要,当迅速而明确的结果对于解决有关产品纯度或与制造问题有关的问题至关重要时...
-
欧代服务_如何选择欧盟授权代表?
产品出口欧盟授权代表要求: 2021年7月之后销往欧洲的产品光是带有CE认证标志也不够,还需贴上“欧代信息”。如果卖家不能遵守相关法规要求,缺失欧代信息的贴标,即将会遭受平台强制下架产品链接以及海关扣押货物的风险。欧盟授权代表(European Authorised Representative 或European Authorized Representative)是指由位于欧洲经济区EEA(包括EU与EFTA)境外的制造商明确指定的一个自然人或法人。该自然人或法人可代表E...
-
第59条和医疗设备的欧洲CE标记
第59条和医疗设备的欧洲CE标记2020年4月23日,修订关于医疗设备(MDR)的法规(EU)2017/745的法规(EU)2020/561规定,该MDR的申请日期延迟了一年,它还修改了该法规的第59条:1.在MDR适用之前,当前的医疗器械指令也将纳入第59条的范围。2.虽然MDR从2021年5月26日开始适用,但第59条将从2020年4月24日开始适用。第59条规定了如何批准医疗器械(非IVD)的CE标记要求减损授权,鉴于COVID-19大流行,为加快投放到欧盟市场的设备的文书工作,可能是有道理的,与此同时,在适...
-
符合欧盟MDR的医疗设备标签要求
医疗设备MDR标签要求 随着欧盟MDR过渡期限越来越近,制造商必须以最高优先级和谨慎性来执行标签要求,并必须确保高标准的质量和合规性,在执行之前,了解新的标签要求和准确的实施至关重要;任何标签错误都可能阻碍进度,导致产品召回并导致代价高昂的延迟。因此,关键是要仔细准备符合EU MDR标签要求的医疗器械标签,例如:欧盟MDR标签要求1.如果没有到期日期,制造商应提供设备的名称和商品名称以及生产日期。2.所有标签都必须具有标准化的符号,该符号表示运入欧盟的包装中包含医疗器械。3....
-
医疗器械ce认证MDR/IVDR公告机构指定了哪些?
全球医疗器械制造商正忙于开展与欧盟《医疗器械法规》(MDR)和《体外诊断法规》(IVDR)有关的合规性计划活动,以分别在2021年5月和2022年5月达到合规性,当然,符合性计划的一部分是与指定给这些法规的公告机构签约,以履行当前和将来的法规义务。更新截至2020年7月10日,共有15个指定为MDR的公告机构,四(4)个指定为IVDR的机构,还有至少九(9)个指定机构正在等待指定,到目前为止,欧盟委员会最近已报告了44份MDR和11份IVDR申请,下面列出了指定的指定机构的当前列表。指定为MDR 2017/745的...